ข้อสอบ o-net
1)
การจัดเรียงอิเล็กตรอนของ 24Cr และ 29Cu ในข้อใดถูกต้อง
ก.

ข.

ค.

ง.

2)
เลขมวลของธาตุชนิดหนึ่งเท่ากับ 60 ธาตุนี้มี 2 ไอโซโทป มีอัตราส่วนเท่ากัน ถ้าธาตุนี้มีเลขอะตอมเท่ากับ 27 จำนวนนิวตรอนของแต่ละไอโซโทปควรเป็นตามข้อใด
ก.
26 และ 28
ข.
33 และ 33
ค.
31 และ 35
ง.
32 และ 33
3)
สารใดมีพลังงานแลตทิช (Lattice energy) มากที่สุด
ก.
NcCl
ข.
MgO
ค.
CaCl2
ง.
AIF3
4)
โมเลกุลใด มี 6 bonding electrons
ก.
C2H4
ข.
CO2
ค.
H2S
ง.
NCI3
5)
สารประกอบข้อใดละลายน้ำได้น้อยที่สุด
ก.
C6H5NH2
ข.
C6H5CO2Na
ค.
CH3CH (OH) CH3
ง.
CH3CH (NH2) CO2H
6)
สมการใดเป็นพลังงาน lattice energy ของสารประกอบไอออนิก XY
ก.
ข.
ค.
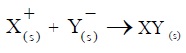
ง.
7)
ข้อใดมีการเปลี่ยนแปลงพลังงานไฮเดรชัน คายความร้อนมากที่สุด
ก.

ข.
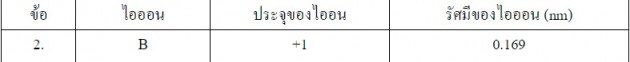
ค.

ง.

8)
ความดันในภาชนะ 10 m3 เป็น 50 kPa และความดันในภาชนะ 30m3 เป็น 100 kPa ถ้านำภาชนะทั้งสองมาต่อกันโดยให้อุณหภูมิคงที่ ความดันในภาชนะรวมจะเป็นเท่าใด
ก.
75 kPa
ข.
87.5 kPa
ค.
125 kPa
ง.
150 kPa
9)
ข้อใดเป็นการเปลี่ยนแปลงพลังงานการเกิดสารประกอบ (the enthalpy change of formation of a compound)
ก.
2H2(g) + O2(g) → 2H2O(g)
ข.
Na(s) + Cl(g) → NaCl(s)
ค.
H2O(l) + NaCl(s) → NaCl(aq)
ง.
K(s) + Mn(s) + 2O2(g) → KMnO4(s)
10)

ก.
-146 kJ.mol-1
ข.
– 140 kJ.mol-1
ค.
+ 140 kJ.mol-1
ง.
+146 kJ.mol-1
11)
สมการแสดงปฏิกิริยาการตกตะกอนอย่างสมบูรณ์เป็นดังนี้
CaCl2(aq) + 2NaOH(aq) → 2NaCl(aq) + Cd(OH)2(s)
เมื่อเติมสารละลาย NaOH เข้มข้น 0.10 โมลต่อลิตร จำนวน 9.0 cm3 ลงในสารละลาย CdCl2 เข้มข้น 1.00 โมลต่อลิตร จำนวน 500 cm3 จะได้ Cd(OH)2 หนักกี่กรัม (มวลอะตอมของ Cd = 112.4, O = 16, H = 1)
CaCl2(aq) + 2NaOH(aq) → 2NaCl(aq) + Cd(OH)2(s)
เมื่อเติมสารละลาย NaOH เข้มข้น 0.10 โมลต่อลิตร จำนวน 9.0 cm3 ลงในสารละลาย CdCl2 เข้มข้น 1.00 โมลต่อลิตร จำนวน 500 cm3 จะได้ Cd(OH)2 หนักกี่กรัม (มวลอะตอมของ Cd = 112.4, O = 16, H = 1)
ก.
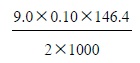
ข.
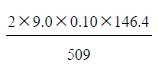
ค.
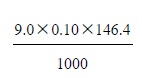
ง.
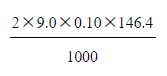
12)
ปฏิกิริยาในข้อใดเป็นปฏิกิริยารีดอกซ์
ก.
CaCO3(s) + 2HCl(ag) → CaCl2(aq) + CO2(g) +H2O(I)
ข.
CuS(s) + O2(g) → Cu(s) + SO2(g)
ค.
Hg(NO3)2(aq) + H2S(g) → HgS(s) + 2HNO3(aq)
ง.
2NaOH(aq) + H2SO4(aq) → Na2SO4(aq) + 2H2O(I)
13)
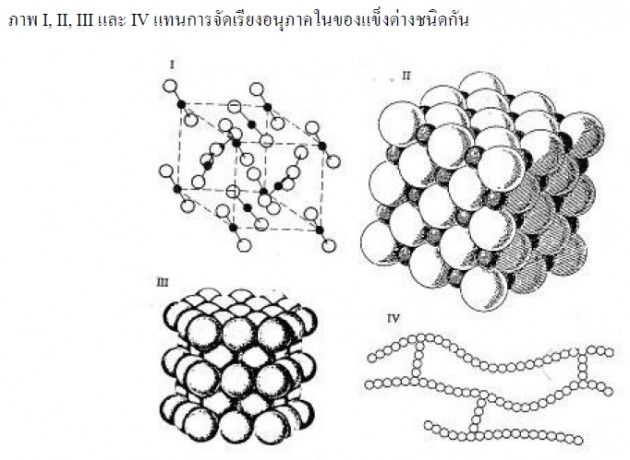
ก.

ข.

ค.

ง.

14)
ข้อใดเป็นโครงสร้างอิเล็กตรอนของอะตอมของธาตุที่มีค่าพลังงานไอออไนเชชันลำดับที่ 1 ถึง 4 ในหน่วย กิโลจูลต่อโมลเป็นดังนี้
I1 = 744, I2 = 1457, I3 = 7739, I4 = 10547
I1 = 744, I2 = 1457, I3 = 7739, I4 = 10547
ก.
2, 3
ข.
2, 7
ค.
2, 8, 2
ง.
2, 8, 8, 1
15)
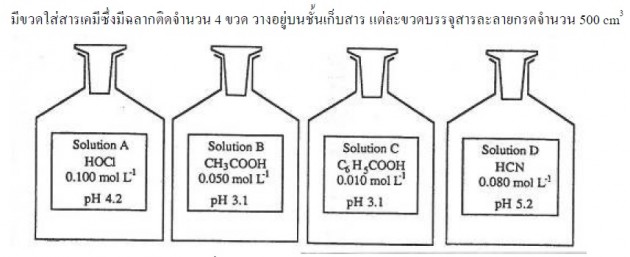 สารละลายกรดในขวดใดเป็นกรดแก่ที่สุด
สารละลายกรดในขวดใดเป็นกรดแก่ที่สุด
ก.
สารละลาย A
ข.
สารละลาย A
ค.
สารละลาย C
ง.
สารละลาย D
16)
ข้อใดมีความหนาแน่นต่ำที่สุด ที่อุณหภูมิ 25°C (298 K) และความดัน 101.3 kPa
ก.
1.0 ลิตรของออกซิเจน
ข.
1.0 ลิตรของนีออน
ค.
1.0 ลิตรของคลอรีน
ง.
1.0 ลิตรของปรอท
17)
กำหนดสูตรของ thorium chloride เป็น ThCI4 และสูตรของ ammonium chromite เป็น NH4CrO2 ข้อใดเป็นสูตรของ thorium chromite
ก.
ThCrO2
ข.
Th2CrO2
ค.
Th(CrO2)4
ง.
Th(CrO2)2
18)
ธาตุแกลเลียมมีสองไอโซโทป คือ 60Ga น้ำหนักอะตอม 68.9 และ 71Ga น้ำหนักอะตอม 70.9 ถ้าธาตุแกลเลียมที่เกิดในธรรมชาติมีน้ำหนักอะตอม 69.7 เศษส่วนของ 69Ga ในแกลเลียมที่เกิดในธรรมชาติเป็นไปตามข้อใด
ก.
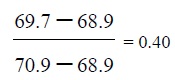
ข.
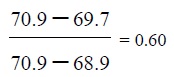
ค.
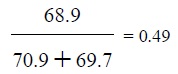
ง.
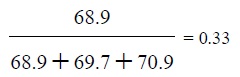
19)
ยา papaverine ใช้รักษา impotence ประกอบด้วยคาร์บอน 70.75% โดยมวล, ไฮโดรเจน 6.25% โดยมวล, ไนโตรเจน 4.13% โดยมวลและออกซิเจน 18.87% โดยมวล ถ้าหนึ่งโมลของ papaverine มีมวล 339.2 กรัม สูตรโมเลกุลของยา papaverine คือข้อใด
ก.
C20H21NO4
ข.
C20H11NO2
ค.
C20H23N2O3
ง.
C17H30NO5
20)
ข้อใดเป็นไอโซเมอร์ของ 2, 2-dimethyl-3elthyl hexane
ก.
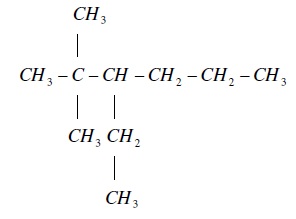
ข.
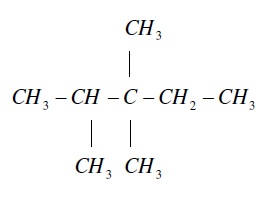
ค.
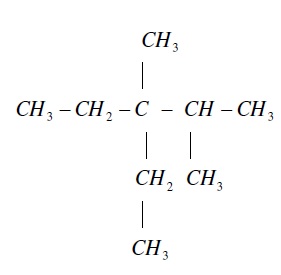

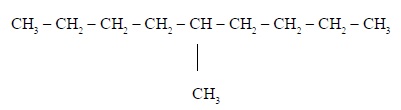
ไม่มีความคิดเห็น:
แสดงความคิดเห็น